26.07.2022
Seltene Mutation führte zu pränataler Blutarmut
Ein Kind, das vor sieben Jahren in Innsbruck zur Welt kam und bereits vor seiner Geburt fünf Blutkonserven benötigte, beschäftigte ein multidisziplinäres Team um Roman Crazzolara und Benjamin Hetzer von der Univ.-Klinik für Pädiatrie I (Direktor: Thomas Müller). In intensiver Forschung, insbesondere in Zusammenarbeit mit Thomas Gruber vom Institut für Zellgenetik (Direktor: Gottfried Baier), ist es den Wissenschafter:innen gelungen, eine Mutation im GATA1 Protein als Ursache der Anämie zu identifizieren und den Mechanismus zu beschreiben.
Der Bub ist heute sieben Jahre alt und gesund. „Es geht ihm gut. Er hat nach dem Auswachsen ein sehr stabiles Blutbild erreicht und benötigt keine Therapie mehr. Das Kind hat vor und nach der Geburt Blutkonserven gebraucht, sonst hat es keine Folgen davongetragen“, sagt Roman Crazzolara. Dennoch war es dem Experten für pädiatrische Hämatologie und Onkologie sowie Erstautor Benjamin Hetzer ein Anliegen, die Blutarmut des Kindes „tiefgründig zu analysieren“.
In Kooperation mit dem CCRI (Children’s Cancer Research Institute) der St. Anna Kinderkrebsforschung in Wien, sowie dem Institut für Humangenetik an der Med Uni Innsbruck (Direktor: Johannes Zschocke), in dem Sequenzierungen vorgenommen wurden, und, allen voran, dank der Unterstützung von Thomas Gruber vom hiesigen Institut für Zellgenetik konnten sie der Anämie auf den Grund gehen. Nach rund einem Jahr Forschungstätigkeit ist es dem Team gelungen, eine seltene, „komplett neue Mutation und den funktionellen Verlust, der damit einhergeht“ nachzuweisen. Aufgrund der Punktmutation R307H in GATA1 kommt es zu einer reduzierten Phosphorylierung (Aktivierung, Anm.) an Ser310. In Fachkreisen wurde bisher die Relevanz dieser Phosphorylierung bei der Erythropoese (Bildung von roten Blutkörperchen, Anm.) im menschlichen Organismus kontrovers diskutiert. In der nun, im Fachjournal Blood Advances publizierten Forschungsarbeit konnte nicht nur die bisher unbekannte Mutation in GATA1 beschrieben werden, sondern auch gezeigt werden, dass die Phosphorylierung an Ser310 in der fetalen Erythropoese eine entscheidende Rolle spielt.
„Wir haben gesehen, dass die Punktmutation zu einer verminderten Aktivität von GATA1 führt und es dadurch zu einem lebensbedrohlichen Mangel an roten Blutkörperchen kommen kann“, wie Crazzolara schildert. Er führte die Forschungsarbeit im Rahmen seiner von der Kinderkrebshilfe gestifteten Professur, die er 2019 angetreten hat, durch.

BU: v.l.: Die Autoren Benjamin Hetzer, Thomas Gruber und Roman Crazzolara (MUI)
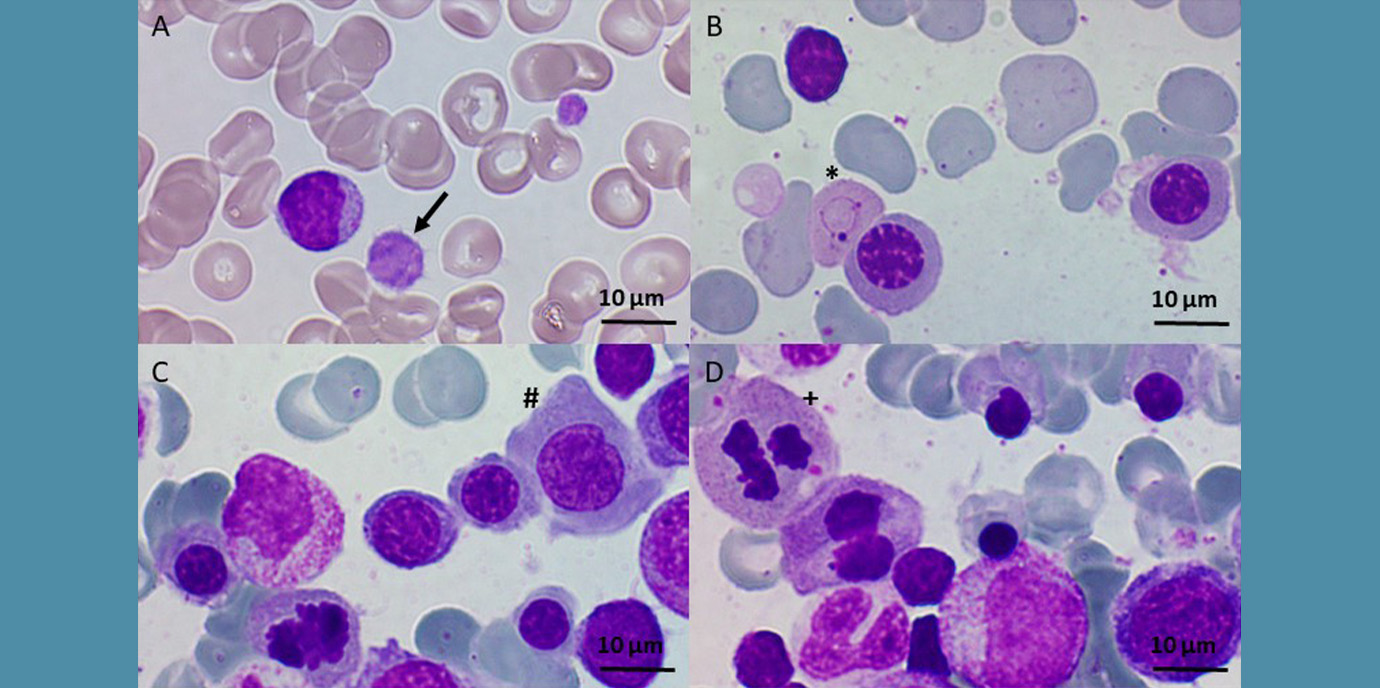
(26.07.2022, Text: T. Mair, Bild Knochenmarksabstrich: Copyright: The American Society of Hematology, Publication: Blood Advances)
Links:
A R307H substituion in GATA1 that prevents S310 phosphorylation causes severe fetal anemia. Benjamin Hetzer et al., Blood Adv (2022) 6 (14): 4330–4334.



