Neuer Antrieb für die nächste Generation von Cochlea-Implantaten
Mit den Erkenntnissen eines Kooperationsprojekts zwischen der TU München und dem Innenohrlabor der HNO-Klinik an der Medizin Uni Innsbruck sollen Cochlea-Implantate einen Entwicklungsschub erfahren. Ausgewiesenes Ziel ist die Verbesserung von Computermodellen, mit denen die gezielte elektrische Stimulation des Hörnervs durch ein Implantat simuliert werden kann. Die Deutsche Forschungsgemeinschaft (DFG) und der Österreichische Wissenschaftsfonds (FWF) fördern das vielversprechende Vorhaben.
Schon seit den 1970er Jahren werden Hörimplantate eingesetzt, um das Hörvermögen und Sprachverstehen von ertaubten und hochgradig schwerhörigen PatientInnen wiederherzustellen. Eine Elektrode wird dazu in die Hörschnecke (Cochlea) eingeführt und ist mit einem Sprachprozessor mit Mikrophonen verbunden, akustische Signale werden so in elektrische Impulse umgewandelt und stimulieren den Hörnerv. Das Implantat ersetzt somit die Funktion der reizwahrnehmenden Haarsinneszellen, von denen der Mensch nur etwa 3.500 besitzt. Schon der Verlust einer einzigen dieser Sinneszellen führt zu einer Einschränkung des Hörvermögens. Mit der Entwicklung von sogenannten Mehrkanalgeräten leisteten australische Forscher sowie das österreichische Ehepaar Ingeborg und Erwin Hochmair vor etwa 30 Jahren Pionierarbeit. „Dieses erfolgreiche bionische Implantat – erstmals wird ein Sinnesorgan durch eine technische Lösung ersetzt – wurde zwischenzeitlich weltweit über eine Million Mal eingesetzt. In den letzten 30 Jahren gab es jedoch kaum wesentliche Verbesserungen und der Therapieerfolg bei Patienten variiert immer noch stark. Die Entwicklung neuer Stimulationsstrategien wird dadurch erschwert, dass eine direkte elektrophysiologische Messung an den Nervenzellen nicht möglich ist. Wir können in unser Hörorgan nicht so einfach ‚hineinschauen‘, da es sich inmitten des Felsenbeines, einem sehr harten Knochen im Schädel, befindet“, erklärt Rudolf Glückert vom Innenohrlabor der Univ.-Klinik für Hals-, Nasen- und Ohrenheilkunde (Direktor: Benedikt Hofauer) die grundlegenden Herausforderungen.
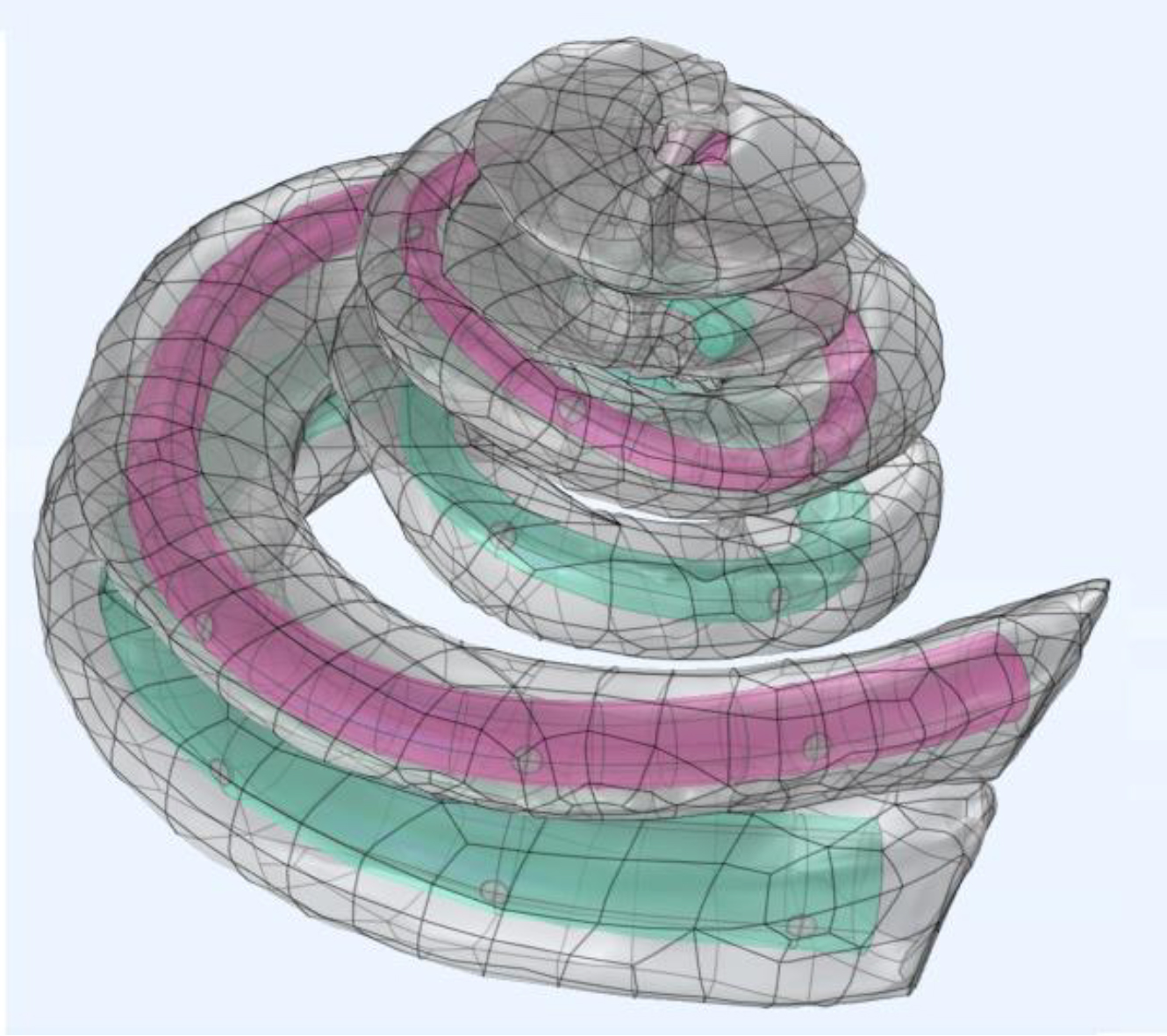
Finetuning für Stimulation und Simulation
Für die Weiterentwicklung von Cochlea-Implantaten wären Computermodelle notwendig, die präzise genug sind, die elektrische Stimulation des Hörnervs punktgenau zu simulieren. Dieses „Finetuning“ hat sich das Projekt „Feinstruktur-basierte Modelle zur Hörimplantat Verbesserung“ – ein Fortsetzungsprojekt einer vorangegangenen Zusammenarbeit – zum Ziel gesetzt. Gelingen soll das in der Kollaboration zwischen den SimulationsexpertInnen Werner Hemmert und Bai Siwei vom Munich Institute of Biomedical Engineering (MIBE) an der TU München und Rudolf Glückert, dessen Expertise in der Erforschung von menschlichen Hörschnecken auf seiner mehr als 20-jährigen Forschungstätigkeit mit histologisch-bildgebenden Verfahren als auch Zell- und Organkulturmodellen beruht. „Nun wollen wir noch mehr Infos in die Modelle packen. Neben zahlreichen hochauflösenden Computertomogrammen zur Erfassung der individuellen Unterschiede der Hörschnecke werden wir tief in die Mikroanatomie des menschlichen Hörnervs blicken und molekulare Komponenten wie die Verteilung von Ionenkanälen quantifizieren, die wichtig sind für die Auslösung und Verarbeitung elektrischer Signale und auch die Verbindungswege zwischen Nervenfasern und Zellkörper kartieren. Pathologische Veränderungen in der Hörschnecke werden hier ebenfalls berücksichtig, da Cochlea-Implantate ja nicht für gesunde Hörende entwickelt werden“, betont Glückert.
Alle neuen Erkenntnisse und Daten werden schließlich in Simulationen der Stromausbreitung und Reizantwort des Hörnervs fließen und mit realen Messungen von Cochlea-Implantat-NutzerInnen verglichen. „Auf diese Weise können wir ganz neue Muster der elektrischen Stimulation testen und Impulse für verbesserte, individualisierte Cochlea-Implantate liefern“, so Glückert.

Nach seinem Studium der Biologie und Biomedizinischen Analytik arbeitet Rudolf Glückert seit dem Jahr 2000 am HNO Forschungslabor für Innenohrbiologie, erlangt 2005 die Doktoratswürde und habilitiert sich 2016. 2023 übernimmt er die Leitung des Innenohrlabors. Zahlreiche Forschungsprojekte erschließen neues Wissen in Ultrastruktur, molekularem Aufbau und Embryonalentwicklung des menschlichen Innenohres. Mit Zell-, Organ- und Tiermodellen forscht Glückert an neuen pharmakologischen Wegen ins Innenohr und an der Regenerationsfähigkeit des Hörnervs. Simulationsmodelle sind seit 15 Jahren ein wichtiges Werkzeug, Erkenntnisse in mathematische Modelle zu gießen und anderen Forschenden zur Verfügung zu stellen.
(31.07.2023.2023, Text: D. Heidegger, Bilder: HNO-Labor, Portrait: Stefan Walser)
Links:
Univ.-Klinik für Hals-, Nasen- und Ohrenheilkunde
Feinstruktur-basierte Modelle zur Hörimplantat Verbesserung




