Das Komplement-System ist nicht „schuld“ an schweren Coronaverläufen
Während ihres Post-Docs in Amsterdam begann Marta Bermejo-Jambrina die Rolle des Komplement-Systems bei Coronainfektionen zu erforschen. Dabei stellte sich heraus, dass nicht nur überschießende Komplementfaktoren zu schweren Verläufen führen, sondern vielmehr das Verhältnis zwischen Komplement- und Antikörperkonzentration von Bedeutung ist. Kürzlich publizierte das Fachjournal EMBO die Ergebnisse der Studie, die Bermejo-Jambrina als postDoc fellow der ÖAW an der Med Uni Innsbruck durchführte.
Das Komplement-System – ein Teil des angeborenen Immunsystems - sei angeblich verantwortlich für Zytokinstürme und daraus resultierende erhöhte Entzündungswerte, die wiederum schwere SARS-CoV-2 Verläufe zur Folge hätten. Ob diese Annahme, die vor allem zu Beginn der Covid-19 -Pandemie verbreitet war, zutrifft, hat ein österreichisch-niederländisches Forschungsteam ab 2022 untersucht. „Basierend auf früheren Publikationen in der Gruppe von Teunis Geijtenbeek an der UMC in Amsterdam haben wir gesehen, dass SARS-CoV-2 Viren unter dem Radar der dendritischen Zellen bleiben. Diese Immunzellen werden nicht aktiviert. Das heißt, sie reifen nicht, weshalb sie den T-Lymphozyten auch keine Antigene präsentieren können. Daher sind wir davon ausgegangen, dass das Komplement-System eine wichtige Rolle spielen muss“, schildert Erst- und co-korrespondierende Autorin Marta Bermejo-Jambrina vom Institut für Hygiene und medizinische Mikrobiologie (Direktorin: Cornelia Lass-Flörl). Das war die Ausgangslage für eine Studie, die vor wenigen Tagen im EMBO Journal (online) veröffentlicht wurde.
Die ForscherInnen untersuchten im Geijtenbeek Labor in den Niederlanden, wie dendritische Zellen des angeborenen Immunsystems mit dem Virus, das von Komplement-Fragmenten markiert/opsonisiert ist, interagieren. Hierfür verwendeten sie Blutkonserven von gesunden Menschen, die bereits vor Ausbruch der Pandemie abgenommen worden waren, als auch Plasma von COVID-19 PatientInnen mit milden und mit schweren Infektionsverläufen, die durch die erste in Europa aufgetretene SARS-CoV-2-Variante (Wildtyp) verursacht wurden. „Es zeigte sich, dass die Zellen sehr gut auf das Virus ansprechen“, sagt Bermejo-Jambrina.
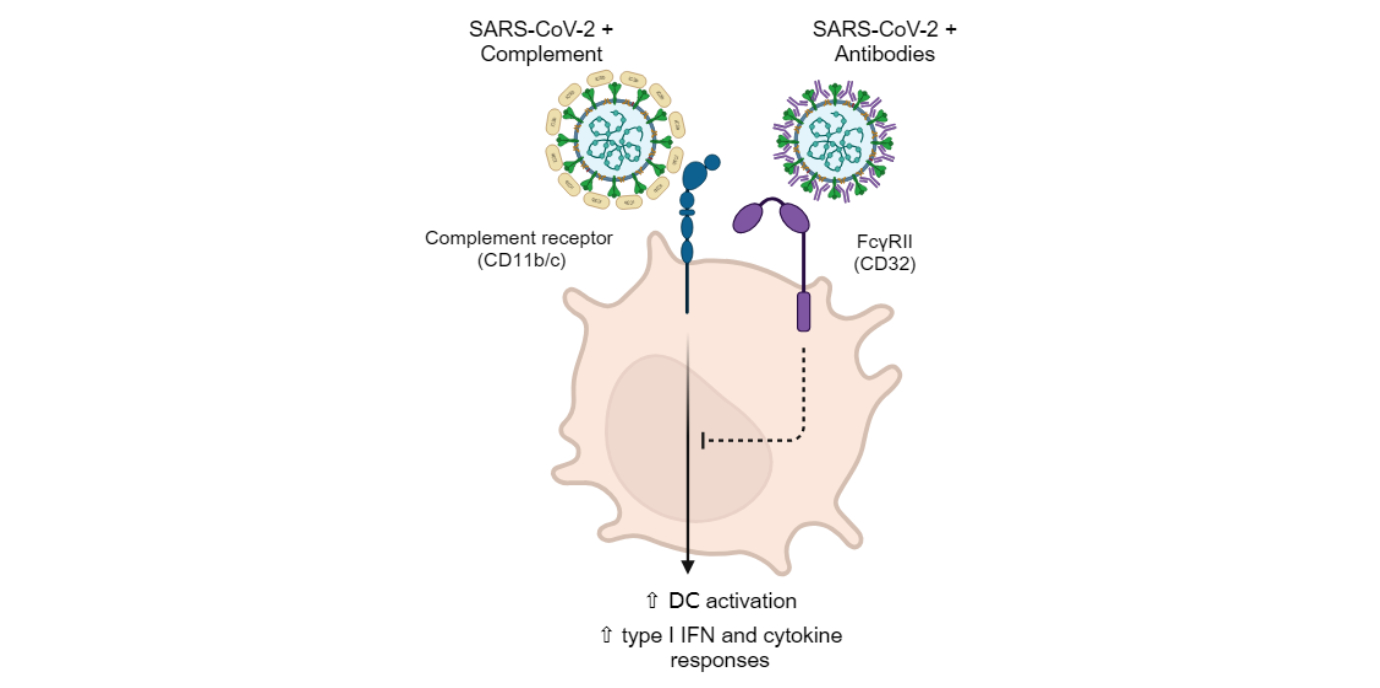
In der Folge wollten die WissenschafterInnen herausfinden, wie das Komplement-System bei schweren Verläufen reagiert. Im Vergleich stellten sie fest, dass sich die Zusammensetzung des Plasmas bei schweren Verläufen von jenem der mild erkrankten PatientInnen unterschied: Die untersuchten Faktoren des Komplement-Systems waren deutlich dysreguliert, was sich auch in den Symptomen und hohen Entzündungswerten widerspiegelte. „Zudem stellte sich heraus, dass in gesundem Blut und in den Proben von PatientInnen mit milden Verläufen ein Gleichgewicht zwischen Komplement- und Antiköperspiegel bestand.“ Das bestätigten auch Folgetests bei denen die ForscherInnen den Antikörperrezeptor (FcɣRII/CD32) blockierten: Die Komplementfaktoren stiegen unkontrolliert an, während ausgleichende Antikörper fehlten. Bermejo-Jambrina schließt daraus, dass das Komplement-System in Bezug auf SARS-CoV-2 nicht per se einen „schlechten“ Einfluss hat, sondern ein ausgewogenes Zusammenspiel von Immunfaktoren wie Komplement und Antikörper notwendig ist.
Ob es sich dabei um neutralisierende oder nicht neutralisierende Antikörper handelt, spiele übrigens keine Rolle. „Der Unterschied ist, dass neutralisierende Antikörper das Virus spezifisch angreifen können, während die nicht neutralisierenden das Virus bloß markieren oder andere Aufgaben übernehmen. Für die Schwere der Entzündung und den Krankheitsverlauf ist das aber nicht bedeutsam.“ Kritische Covid-Verläufe bei Ausbruch der Pandemie erklärt sie sich damit, dass Antikörper möglicherweise noch in unzureichender Menge oder fehlerhaft gebildet wurden Untersuchungen anderer Forschungsgruppen hätten etwa ergeben, dass die Glykosylierung der Antikörper anfangs noch mangelhaft war.
Ob die Studienergebnisse auch für Viren gelten, die SARS-CoV-2 ähnlich sind, müsse in weiteren Forschungsprojekten geklärt werden. Bermejo-Jambrina kann sich jedenfalls vorstellen, dass einige der Erkenntnisse auch für die weitere Forschung an chronisch entzündlichen Autoimmunerkrankungen, wie beispielsweise rheumatoide Arthritis, relevant sein könnten.

Marta Bermejo-Jambrina startete die Forschungsarbeit im Rahmen ihres dreijährigen Post-Doc-Studiums mit KollegInnen in Amsterdam. Ein APART-MINT Stipendium der Österreichischen Akademie der Wissenschaften (ÖAW) ermöglichte ihr im Oktober 2022 die Rückkehr nach Innsbruck und die Weiterführung des Projekts am Institut für Hygiene und medizinische Mikrobiologie im Labor von Doris Wilflingseder, wo sie bereits ihr PhD-Studium erfolgreich absolviert hatte. Bevor sie nach Österreich kam, studierte die Spanierin in Sevilla und in Deutschland Biochemie.
(Innsbruck, 27. März 2024, Text: T. Mair, Bilder: EMBO, privat)
Forschungsarbeit:
Bermejo-Jambrina M., Van der Donk L., Van Hamme J., Wilflingseder D et. al.: Control of complement-induced inflammatory responses to SARS-CoV-2 infection by anti-SARS-CoV-2 antibodies, EMBO J. 2024 Feb 28. doi: 10.1038/s44318-024-00061-0 https://doi.org/10.1038/s44318-024-00061-0